Ліки від а до я -
Хвороби -
Калькулятор калорій -
Магнітні бурі -
Дієти -
Очищення організму -
Схуднення -
Молочниця
Геморой -
Лікування -
Косметологія -
Поради -
Інсульт -
Інфаркт -
Діабет -
Варикоз -
Вправи -
Covid-19
Ліки та препарати
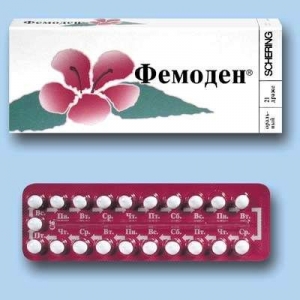
Фемоден
Шерінг АГ, Німеччина
Інструкція
Загальна характеристика:
основні фізико-хімічні властивості: драже білого кольору;
склад: 1 драже містить етинілест радіолу 30 мкг та гестодену 75 мкг;
допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, полівідон 25000, кальцію натрію едетат, магнію стеарат, сахароза, полівідон 700000, полі етиленгліколь 6000, кальцію карбонат, тальк, віск монтангліколевий.
Форма випуску. Драже.
Фармакотерапевтична група. Гормони статевих залоз. Код АТС GO3A A10.
Фармакологічні властивості.
Фармакодинаміка. Контрацептивна дія комбінованих пероральних контрацептивів далі-(КПК) базується на взаємодії різних факторів, найважливішими з яких є супресія овуляції і зміна церві кальної секреції. Окрім захисту від вагітності, КПК мають ще низку позитивних властивостей, які можуть бути застосовані при виборі методу контрацепції. Менструальний цикл стає регулярнішим, менструація зазвичай менш болючою, зменшується крововтрата. Останнє сприяє зниженню частоти залізо дефіцитної анемії. Існують докази зниження ризику раку ендометрія і раку яєчників. Крім того, було доведено, що при застосуванні високо дозованих КПК (50 мкг етінілест радіолу) знижується ризик виникнення кіст яєчників, запальних захворювань органів таза, доброякісних захворювань молочних залоз і позаматкової вагітності. Необхідно з’ясувати, чи стосується це низько дозованих КПК.
Фармакокінетика.
Гестоден
Адсорбція
Після перорального прийому гестоден швидко і повністю всмоктується. Пікова концентрації у сироватці, що становить 4 нг/мл, досягається приблизно через 1 годину після одноразового прийому. Біодоступність складає близько 99%.
Розподіл
Гестоден зв’язується із сироватковим альбуміном і глобуліном, це гормон що зв’язує статеві гормони (ГЗСГ). Лише 1 - 2% від загальної концентрації у сироватці присутні у вигляді вільного стероїду, а 50 - 70% специфічно зв’язані з ГЗСГ. Індуковане етинілестрадіолом підвищення рівня ГЗСГ зумовлює збільшення фракції гестодену, зв’язаної з ГЗСГ фракції і зниження фракції зв’язаної з альбуміном.
Метаболізм
Метаболізм гестодену повністю відбувається відомими шляхами метаболізму стероїдів. Кліренс із сироватки становить 0,8 мл/хв/кг.
Виведення з організму
Рівень гестодену в сироватці знижується у дві фази. Розподіл у кінцевій фазі характеризується періодом напів виведення, що дорівнює 12 - 15 год. Гестоден не екскретується у незміненому вигляді. Його метаболіти виводяться з організму із сечею та жовчю у співвідношенні приблизно 6 : 4. Період напі виведення метаболітів становить майже один день.
Стан рівноваги
На фармакокінетику гестодену впливає рівень ГЗСГ, який зростає втричі при одночасному прийомі етинілест радіолу. Після щоденного прийомання рівень гестодену в сироватці зростає приблизно у 4 рази, досягаючи стану рівноваги у другій половині курсу приймання драже.
Етинілестрадіол
Адсорбція
При пероральному прийманні етинілестрадіол швидко і повністю всмоктується. Пікова концентрація у сироватці, що становить приблизно 80 пкг/мл, досягається протягом 1 - 2 год.
Розподіл
Етинілестрадіол міцно, але не специфічно зв’язується з сироватковим альбуміном (приблизно 98%) і збільшує сироваткову концентрацію ГЗСГ.
Метаболізм
Етинілестрадіол метаболізується головним чином шляхом ароматичного гідроксилювання, проте додатково утворюється велика кількість гідроксильованих і м етильованих метаболітів, серед яких існують як вільні метаболіти, так і як кон’югати з глюкуронідами і сульфатами. Кліренс становить 2,3 - 7 мл/хв/кг.
Виведення з організму
Рівень етинілест радіолу в сироватці знижується за дві фази з періодами напів виведення приблизно 1 год і 10 - 20 год, відповідно. Речовина не виводиться з організму у незмінному вигляді, метаболіти етинілест радіолу виводяться з сечею і жовчю у співвідношенні 4:6. Період напів виведення метаболітів становить приблизно один день.
Стан рівноваги
Відповідно до варіабельного часу напів виведення із сироватки і щоденним прийомом рівноважна концентрація етинілест радіолу у сироватці досягається приблизно через тиждень.
Показання для застосування. Контрацепція.
Спосіб застосування і дози.
Як приймати препарат Фемоден
Драже слід приймати щоденно згідно порядку, зазначеному на блістері, приблизно в один і той же час, запиваючи невеликою кількістю рідини. Препарат приймають по 1 драже на добу протягом 21 дня. Приймання драже з кожної наступної упаковки слід розпочинати після закінчення 7-денної перерви у прийманні препарату, під час якої зазвичай відбувається менструальноподібна кровотеча. Як правило, вона починається на 2 - 3-й день після приймання останнього драже і може не закінчитися до початку приймання драже з наступної упаковки.
Як починати приймання препарату Фемоден
Гормональні контрацептиви в попередній період (минулий місяць) не використовувались
Приймання драже слід розпочинати в перший день природного циклу жінки (тобто в перший день менструальної кровотечі). Можна почати прийом і з 2 - 5-го дня, однак у такому випадку протягом першого циклу рекомендується додатково використовувати бар'єрний метод контрацепції протягом перших 7 днів приймання препарату.
Перехід з іншого комбінованого перорального контрацептиву (КПК)
Бажано, щоб жінка почала приймати Фемоден на наступний день після прийому останньої активної таблетки попереднього КПК, принаймні, не пізніше наступного дня після перерви у прийомі таблеток або після прийому таблеток плацебо її попереднього КПК.
Перехід з методу, що базується на застосуванні лише прогестогену (міні-пілі, ін'єкції, імпланти) або внутрішньо маткової системи з прогестогеном
Жінка може розпочати приймання препарату Фемоден в будь-який день після припинення прийому міні-пілі (у випадку імпланту або внутрішньо маткової системи – в день їх видалення, у випадку ін'єкції - замість наступної ін'єкції). Однак у всіх випадках рекомендується додатково використовувати бар'єрний метод контрацепції протягом перших 7 днів приймання драже.
Після аборту в першому триместрі вагітності
Жінка може розпочинати прийом препарату Фемоден негайно. У такому разі у неї немає необхідності застосовувати додаткові засоби контрацепції.
Після пологів або аборту в другому триместрі вагітності.
У випадку годування груддю, див. підрозділ Вагітність та лактація.
Жінкам необхідно рекомендувати розпочинати приймання препарату Фемоден з 21 - 28-го дня після пологів або аборту у другому триместрі вагітності. При пізнішому початку приймання драже додатково слід використовувати бар'єрний метод контрацепції протягом перших 7 днів приймання препарату. Однак, якщо статевий акт уже відбувся, то перед початком використання КПК слід виключити можливу вагітність, або жінці слід дочекатися менструації.
Що робити у випадку пропуску прийому драже
Якщо запізнення в прийманні драже не перевищує 12 год, протизаплідна дія препарату не знижується. Пропущене драже треба прийняти якомога швидше. Наступне драже з цієї упаковки слід приймати у звичний час.
Якщо запізнення з прийомом забутого драже перевищує 12 год, контрацептивний захист може знизитися. У такому разі можна керуватися двома основними правилами:
приймання драже ніколи не можна переривати більш ніж на 7 днів,
адекватне пригнічення системи гіпоталамус-гіпофіз-яєчники досягається безперервним прийманням драже протягом 7 днів.
Відповідно до цього у повсякденному житті слід керуватися нижчезазначеними рекомендаціями:
1-й тиждень
Жінка повинна прийняти останнє пропущене драже якомога швидше, навіть якщо доведеться прийняти два драже одночасно. Після цього вона продовжує приймати драже у звичний час. Крім того, протягом наступних 7 днів слід використовувати бар'єрний метод контрацепції, наприклад презерватив. У разі, якщо у попередні 7 днів відбувся статевий акт, слід враховувати можливість виникнення вагітності. Чим більше драже пропущено і чим ближче перерва у прийомі препарату, тим більше ризик вагітності.
2-й тиждень
Жінка повинна прийняти останнє пропущене драже якомога швидше, навіть якщо доведеться прийняти два драже одночасно. Після цього вона продовжує приймати драже у звичний час. За умови, що жінка правильно приймала драже протягом 7 днів перед першим пропуском, то немає необхідності використовувати додаткові протизаплідні засоби. В іншому разі або при пропуску більш ніж одного драже, рекомендується додатково використовувати бар'єрний метод контрацепції протягом 7 днів.
3-й тиждень
Ризик зниження надійності зростає при наближенні перерви у приймання драже. Однак, при дотриманні схеми приймання драже можна уникнути зниження контрацептивного захисту. Якщо дотримуватися одного з нижченаведених варіантів, то не виникне необхідності використання додаткових контрацептивних засобів за умови правильного приймання драже протягом 7 днів до пропуску. Якщо це не так, слід дотримуватися першого з нижченаведених варіантів і використовувати додаткові методи контрацепції протягом наступних 7 днів.
Жінка повинна прийняти останнє пропущене драже якомога швидше, навіть якщо доведеться прийняти два драже одночасно. Після цього вона продовжує приймати драже у звичайний час. Драже з наступної упаковки слід почати приймати відразу ж після закінчення попередньої, тобто не повинно бути перерви між упаковками. Малоймовірно, що у жінки розпочнеться менструальноподібна кровотеча до закінчення прийому другої упаковки, хоча під час прийому драже може спостерігатися кровомазання або проривна кровотеча.
Жінці можна також порадити припинити приймання драже з використовуваної упаковки. В такому випадку перерва у прийомі препарату повинна складати до 7 днів, включаючи дні пропуску драже; прийом драже слід почати з наступної упаковки.
Якщо жінка пропустила приймання драже, і у неї відсутня менструальноподібна кровотеча під час першої звичайної перерви у прийманні драже, слід розглянути ймовірність вагітності.
Рекомендації у випадку розладів з боку шлунково-кишкового тракту
У випадку тяжких розладів з боку шлунково-кишкового тракту можливе неповне всмоктування препарату; у такому разі слід застосовувати додаткові засоби контрацепції.
Якщо протягом 3 - 4 годин після прийому драже сталося блювання, доцільно скористатися рекомендаціями щодо пропуску прийому драже. Якщо жінка не хоче змінювати свою звичайну схему приймання препарату, їй необхідно прийняти додаткову таблетку (и) з іншої упаковки.
Як змінити час виникнення менструації або як затримати менструацію
Щоб затримати виникнення менструації, жінці слід продовжувати приймати драже Фемоден із нової упаковки і не робити перерви у прийманні препарату. За бажанням, термін прийому можна продовжити аж до закінчення другої упаковки. При цьому не можна виключити проривну кровотечу або кровомазання. Звичайне приймання препарату Фемоден відновлюється після 7-денної перерви в прийомі драже.
Щоб змістити час настання менструації на інший день тижня, рекомендується скоротити перерву в прийомі драже на стільки днів, на скільки бажано. Слід зазначити, що чим коротшою буде перерва, тим частіше спостерігається відсутність менструальноподібної кровотечі та проривна кровотеча або кровомазання протягом прийому драже з другої упаковки (як і у випадку затримки настання менструації).
Побічна дія. Серйозніші побічні ефекти, пов’язані з використанням КПК, описані в розділі Особливості застосування.
Повідомлялося про інші небажані ефекти при застосуванні КОК, однак їх зв'язок з прийманням КПК не був ані підтверджений, ані спростований:
Органи та системи Часті
(≥ 1/100) Нечасті
(≥1/1000 і (< 1/1000)
Органи зору непереносимість контактних лінз
Шлунково-кишковий тракт нудота, абдомінальний біль блювання, діарея
Імунна система гіпер чутливість
Дослідження Збільшення маси тіла зменшення маси тіла
Обмін речовин та порушення харчування затримка рідини
Нервова система головний біль мігрень
Психічні розлади пригнічений настрій, зміна настрою зниження лібідо підвищення лібідо
Репродуктивна система та молочні залози Болючість молочних залоз, відчуття напруженості молочних залоз збільшення молочних залоз Зміни вагінальної секреції, поява секреції із молочних залоз
Шкіра та підшкірні тканини висипання, кропив’янка вузлувата еритема, ексудативна мультиформна еритема
Протипоказання. Комбіновані пероральні контрацептиви (КПК) не повинні використовуватися за наявності жодного із нижчезазначених станів або захворювань. У разі, якщо будь-який із цих станів або захворювань виникає вперше під час застосування КПК, прийом препарату слід негайно припинити.
Венозні або артеріальні тромботичні/тромбоемболійні явища (наприклад, тромбоз глибоких вен, легенева емболія, інфаркт міокарда) або це ребро-васкулярний розлад нині або в анамнезі.
Наявність нині або в анамнезі продромальних симптомів тромбозу (наприклад, транзиторне порушення мозкового кровообігу, стенокардія).
Мігрень з вогнищевими неврологічними симптомами в анамнезі.
Цукровий діабет з ураженням судин.
Наявність тяжких або множинних факторів ризику щодо венозного або артеріального тромбозу також може стати протипоказанням (див. розділ Особливості застосування).
Панкреатит нині або в анамнезі, якщо він пов’язаний із тяжкою гіпертри гліцеридемією.
Наявність нині або в анамнезі тяжких захворювань печінки, поки показники функції печінки не повернуться до нормальних значень.
Наявність нині або в анамнезі пухлин печінки (доброякісних або злоякісних).
Відомі або підозрювані злоякісні пухлини (наприклад, статевих органів або молочних залоз), що є залежними від статевих гормонів.
Вагінальна кровотеча нез’ясованої етіології.
Відома чи підозрювана вагітність.
Підвищена чутливість до діючих речовин або до будь-якого із компонентів препарату.
Передозування. Про серйозні негативні ефекти внаслідок передозування не повідомлялось. Можуть спостерігатись такі симптоми передозування: нудота, блювання, а у молодих дівчат - незначна кровотеча із піхви. Жодних антидотів не існує, лікування повинно бути симптоматичним.
Особливості застосування. За наявності будь-якого із зазначених нижче станів/факторів ризику користь від застосування КПК повинна бути виважена проти можливого ризику з урахуванням індивідуальних особливостей кожної пацієнтки та обговорена з жінкою до того, як вона вирішить приймати КПК. При загостренні, погіршенні або першому виникненні будь-якого із зазначених нижче станів або факторів ризику жінці рекомендується звернутися до лікаря. Лікар повинен прийняти рішення, чи слід припинити застосування КПК.
Циркуляторні порушення
На підставі результатів епідеміологічних досліджень припускається існування зв’язку між застосуванням КПК та підвищенням ризику виникнення венозних та артеріальних тромботичних і тромбоемболічних захворювань, таких як інфаркт міокарда, інсульт, тромбоз глибоких вен та емболія легеневої артерії. Наведені стани виникають рідко.
Венозна тромбоемболія (ВТЕ), що проявляється у вигляді венозного тромбозу та/або легеневої емболії, може виникнути при використанні будь-якого КПК. Ризик виникнення венозної тромбоемболії є вищим протягом першого року застосування КПК. Частота ВТЕ у жінок, які приймають пероральні контрацептиви з низькою дозою естрогенів (< 0,05 мг етинілест радіолу) становить до 4 випадків на 10000 жінок/рік порівняно з 0,5 - 3 випадків на 10000 жінок/рік у тих жінок, які не використовують пероральні контрацептиви. Частота ВТЕ, асоційована з вагітністю, складає 6 випадків на 10 000 жінок/рік.
Надзвичайно рідко повідомлялось про виникнення тромбозу в інших кровоносних судинах, наприклад артеріях і венах печінки, нирок, мезентеріальних судинах, судинах головного мозку або сітківки у жінок, які застосовують КПК. Стосовно зв'язку цих ускладнень з використанням КПК єдиної думки не існує.
Симптомами венозних або артеріальних тромботичних/тромбоемболічних явищ або інсульту можуть бути: однобічний біль у нижніх кінцівках або їх набряк; раптовий сильний біль у грудях, що може віддавати в ліву руку; раптова задишка; кашель, що раптово почався; будь-який незвичний, сильний, тривалий головний біль; раптове зниження або повна втрата зору; диплопія; порушення мовлення або афазія; вертиго; колапс з парціальним епілептичним нападом або без нього; слабкість або дуже виражене раптове оніміння одного боку або однієї частини тіла; порушення моторики; ² гострий² живіт.
Фактори, що підвищують ризик виникнення венозних або артеріальних тромботичних/тромбоемболічних явищ або інсульту:
вік;
паління (у поєднанні з інтенсивним палінням і підвищенням віку ризик зростає, особливо у жінок після 35 років);
сімейний анамнез (наприклад, випадки венозної або артеріальної тромбоемболії у братів чи сестер або батьків у відносно ранньому віці). Якщо підозрюється спадкова схильність, перед вирішенням питання про використання будь-якого КПК, жінка повинна бути направлена на консультацію до відповідного фахівця;
ожиріння (індекс маси тіла більше 30 кг/м2);
дисліпопротеїнемія;
гіпертензія;
мігрень;
захворювання клапанів серця;
фібриляція передсердь;
тривала іммобілізація, радикальні хірургічні втручання, будь-які хірургічні операції на нижніх кінцівках, значні травми. В цих випадках рекомендується припинити використання КПК (при планових операціях як найменше за чотири тижні до її проведення) і не починати знову його прийом раніше 2 тижнів після повної ре мобілізації.
Немає єдиної думки щодо можливої ролі варикозних вен і поверхневого тромбофлебіту у розвитку венозної тромбоемболії.
Необхідно брати до уваги підвищення ризику розвитку тромбоемболії у післяпологовому періоді.
До інших захворювань, які можуть бути пов’язані з серйозними циркуляторними розладами, належать: цукровий діабет; системний червоний вовчак; гемолітичний уремічний синдром; хронічні запальні захворювання кишечнику (хвороба Крона або виразковий коліт) та серпоподібно-клітинна анемія.
Підвищення частоти випадків виникнення мігрені або її загострення під час використання КПК (що може бути передвісником порушення мозкового кровообігу) може вимагати термінового припинення використання КПК.
Біохімічні показники, які можуть бути характерними при спадковій або набутій схильності до венозних або артеріальних тромбозів включають: резистентність до активованого протеїну С (АРС), гіпергомо цистеїнемію, дефіцит анти тромбіну ІІІ, дефіцит протеїну С, дефіцит протеїну S, антифосфоліпідні антитіла (антикардіоліпінові антитіла).
Аналізуючи співвідношення ризик/користь, лікар повинен враховувати той факт, що адекватне лікування станів, про які згадувалося вище, може знижувати пов’язаний з ними ризик виникнення тромбозів, а також і те, що ризик виникнення тромбозів, асоційованих з вагітністю, вищий, ніж при використанні низько дозованих КПК (<0,05 мг етинілест радіолу).
Пухлини
Найважливіший фактор ризику розвитку раку шийки матки є персистенція папіломовірусу. Результати деяких епідеміологічних досліджень вказують на додаткове підвищення ризику розвитку раку шийки матки при довго тривалому використанні КПК, проте це твердження все ще суперечливе, оскільки остаточно не з’ясовано наскільки результати досліджень враховують супутні фактори ризику, наприклад, взяття мазка із шийки матки та статеву поведінку, включаючи застосування бар’єрних методів контрацепції.
Мета-аналіз на підставі 54 епідеміологічних досліджень вказує на незначне підвищення відносного ризику (ВР = 1,24) розвитку раку молочної залози у жінок, які застосовують КПК. Цей підвищений ризик поступово зникає протягом 10 років після закінчення приймання КПК. Оскільки рак молочної залози у жінок молодше 40 років зустрічається рідко, збільшення кількості випадків діагностики раку молочної залози у жінок, що використовують у даний час або нещодавно використовували КПК, є незначним щодо загального ризику раку молочної залози. Результати даних досліджень не надають доказів існування причинного взаємозв’язку. Під вишення ризику може бути обумовлене як більш ранньою діагностикою раку молочної залози у жінок, які використовують КПК, так і біологічною дією КПК або поєднанням обох факторів. Відмічено тенденцію, що рак молочної залози, виявлений у жінок, які коли-небудь приймали КПК, клінічно менш виражений, ніж у тих, хто ніколи не вживав КПК.
У поодиноких випадках у жінок, які застосовують КПК, спостерігалися доброякісні, а ще рідше – злоякісні пухлини печінки, які у поодиноких випадках призводили до небезпечної для життя внутрішньочеревної кровотечі. У випадку виникнення скарг на сильний біль в епігастральній ділянці, збільшення печінки або ознаки внутрішньочеревної кровотечі при диференційній діагностиці слід враховувати можливість наявності пухлини печінки у жінок, які приймають КПК.
Інші стани
Жінки з гіпертри гліцеридемією або сімейним анамнезом цього порушення становлять групу ризику розвитку панкреатиту при вживанні КПК.
Хоча повідомлялося про незначне підвищення артеріального тиску у багатьох жінок, що приймають КПК, клінічно значуще підвищення артеріального тиску є поодиноким явищем. Проте, якщо тривала клінічно виражена гіпертензія виникає під час приймання КПК, то буде слушним відмінити КПК та лікувати гіпертензію. Якщо це доцільно, використання КПК може бути відновлено після досягнення нормотонії за допомогою антигіпертензивної терапії.
Повідомлялось про виникнення або загострення зазначених нижче захворювань під час вагітності та при використанні КПК, але їх взаємозв'язок з використанням КПК не є остаточно з’ясованим: жовтуха та/або свербіж, пов’язаний з холестазом, утворення жовчних каменів, порфірія, системний червоний вовчак, гемолітико-уремічний синдром, хорея Сіденгама, герпес вагітних, втрата слуху, пов’язана з отосклерозом.
При гострих або хронічних порушеннях функції печінки може виникнути необхідність припинити приймання КПК, доки показники функції печінки не повернуться до нормальних значень. При рецидиві холестатичної жовтяниці, що вперше виникла під час вагітності або попереднього приймання статевих гормонів, приймання КПК слід припинити.
Хоча КПК можуть впливати на периферійну інсулінорезистентність та толерантність до глюкози, немає даних щодо потреби змінювати терапевтичний режим у жінок з діабетом, які приймають низько дозовані КПК (що містять < 0,05 мг етинілест радіолу). Проте жінки, які страждають на цукровий діабет повинні ретельно обстежувати ся протягом приймання КПК.
Хвороба Крона та виразковий коліт можуть бути пов’язані з вживанням КПК.
Іноді може виникати хлоазма, особливо у жінок з хлоазмою вагітних в анамнезі. Жінки, схильні до виникнення хлоазми, повинні уникати дії прямих сонячних променів або ультрафіолетового опромінювання під час приймання КПК.
Медичне обстеження
Перед початком або відновленням приймання препарату Фемоден слід провести повне медичне обстеження та докладно вивчити анамнез пацієнтки, беручи до уваги протипоказання (розділ Протипоказання) і застереження (розділ Особливості застосування). При застосуванні КПК рекомендують періодичні обстеження. Проведення таких періодичних обстежень є важливим, оскільки протипоказання (наприклад, транзиторне порушення кровообігу і т. д.) або фактори ризику (наприклад, сімейний анамнез венозного або артеріального тромбозу) можуть вперше виникнути вже під час приймання КПК. Частота і характер цих обстежень повинні ґрунтуватися на існуючих нормах медичної практики з урахуванням індивідуальних особливостей кожної жінки, проте, як правило, особливу увагу приділяють обстеженню тазових органів, включаючи стандартний аналіз цитології шийки матки, органів черевної порожнини, молочних залоз, виміру артеріального тиску.
Необхідно попередити жінку, що пероральні контрацептиви не захищають від ВІЛ-інфекції (СНІДу) та інших захворювань, що передаються статевим шляхом.
Зниження ефективності
Ефективність комбінованих пероральних контрацептивів може знижуватись у випадку пропуску таблетки, розладів шлунково-кишкового тракту або використання інших лікарських засобів.
Контроль циклу
При прийманні пероральних контрацептивів можуть спостерігатися між менструальні кровотечі (кровомазання або проривні кровотечі), особливо протягом перших кількох місяців. Зважаючи на це, обстеження при появі будь-якої між менструальної кровотечі, слід проводити тільки після періоду адаптації організму до препарату, що складає приблизно три цикли.
Якщо порушення циклу продовжуються або поновлюються після декількох нормальних циклів, слід розглянути питання про негормональні причини кровотеч і провести відповідні обстеження з метою виключення наявності пухлин та вагітності. До діагностичних заходів можливо включення кюретаж.
У деяких жінок може не настати менструальноподібна кровотеча під час перерви в прийомі препарату. У разі, приймання КПК відповідно до вказівок, вагітність малоймовірна. Проте, якщо прийом контрацептиву відбувався нерегулярно, або якщо менструальноподібні кровотечі відсутні протягом двох циклів перед продовженням приймання КПК необхідно виключити вагітність.
Вагітність та лактація
Препарат є протипоказаним до застосування у період вагітності. У разі виникнення вагітності під час застосування Фемодену, приймання препарату необхідно припинити. Проте результати епідеміологічних досліджень не вказують на підвищення ризику появи вроджених вад у дітей, якіщо народились від жінок, що приймали КПК до вагітності, так само як і на існування тератогенної дії при ненавмисному прийомі КПК у ранні терміни вагітності.
КПК можуть впливати на лактацію, оскільки під їх впливом може зменшуватись кількість грудного молока, а також змінюватись його склад. Зважаючи на це, КПК не рекомендується приймати при грудному вигодовуванні.
Діючі речовини, що входять до складу препарату, та/або їх метаболіти у невеликих кількостях виділяються з грудним молоком, але немає даних, що це негативно впливає на здоров’я немовляти.
Вплив на здатність керувати автомобілем і працювати з механізмами
Не спостерігалося жодного впливу на здатність керувати автомобілем і працювати з механізмами.
Взаємодія з іншими лікарськими засобами. Взаємодія пероральних контрацептивів та інших лікарських засобів може призводити до проривної кровотечі та/або втрати ефективності контрацептиву. В літературі повідомляється про нижчезазначені взаємодії.
Печінковий метаболізм: може спостерігатися взаємодія з лікарськими препаратами, що індукують мікросомальні ферменти, що може спричинювати зростання кліренсу статевих гормонів (наприклад, фенітоїн, барбітурати, примідон, карбамазепін, рифампіцин і можливо також окскарбазепін, топірамат, фельбамат, ритонавір, гризеофульвін та лікарські засоби, що містять Hypericum perforatum L).
Взаємодія з ентерогепатичною циркуляцією: результати деяких клінічних досліджень дають припущення, що ентерогепатична циркуляція естрогенів може знижуватися при прийманні певних антибіотиків, що можуть знижувати концентрацію етинілест радіолу (наприклад, антибіотики пеніцилінового і тетрациклінового ряду).
При лікуванні будь-яким із наведених вище препаратів жінка повинна тимчасово застосовувати бар'єрний метод додатково до прийому КПК або обрати інший метод контрацепції. При лікуванні препаратами, що індукують мікросомальні ферменти, бар'єрний метод слід застосовувати протягом всього терміну лікування відповідним препаратом і ще протягом 28 днів після припинення його прийому. При лікуванні антибіотиком (за винятком римфапіцину і гризеофульвіну) бар'єрний метод слід використовувати ще протягом 7 днів після його відміни. У разі, якщо бар'єрний метод все ще застосовується, а драже в упаковці КПК уже закінчились, прийом драже з наступної упаковки слід починати без звичайної перерви.
Пероральні контрацептиви можуть впливати на метаболізм інших препаратів. Зважаючи на це, можуть змінюватися концентрації діючих речовин у плазмі та тканинах (наприклад, циклоспорину).
Примітка: Для встановлення потенційної можливості взаємодії з лікарськими засобами, що призначаються одночасно з КПК, рекомендується ознайомитися з інструкціями для медичного застосування цих препаратів.
Вплив на результати лабораторних досліджень
Приймання контрацептивів може вплинути на результати певних лабораторних аналізів, в тому числі на біохімічні параметри функції печінки, щитоподібної залози, наднирників та нирок, показники вмісту в плазмі білків-(носіїв), таких як глобулін, що зв'язує статеві гормони і фракції ліпідів/ліпопротеїнів, параметри вуглеводного обміну, а також параметри коагуляції і фібринолізу. Зазвичай такі зміни перебувають у межах норми.
Умови та термін зберігання. Зберігати при температурі не вище 30º С, в недоступному для дітей місці. Термін придатності – 5 років.
Умови відпуску. За рецептом
Упаковка. Блістер із 21 драже в картонній коробці.
Заявник. Schering AG ( Шерінг АГ).
Адреса. D-13342 Berlin, Germany - Німеччина
| Кількість переглядів: |